Do, 22.09.2022 — Peter Tessarz 
Wenn wir altern, werden unsere Knochen dünner, wir erleiden häufiger Knochenbrüche und es können Krankheiten wie Osteoporose auftreten. Schuld daran sind unter anderem alternde Stammzellen im Knochenmark, die nicht mehr effektiv für Nachschub für das Knochengewebe sorgen. Peter Tessarz und sein Team am Max-Planck-Institut für Biologie des Alterns (Köln) haben jetzt herausgefunden, dass sich diese Änderungen zurückdrehen lassen, und zwar durch die Verjüngung des Epigenoms. Eine solcher Ansatz könnte in Zukunft zur Behandlung von Krankheiten wie Osteoporose beitragen*
Das Epigenom verändert sich in alternden Stammzellen
Viele Alternsforscher haben bereits seit einiger Zeit die Epigenetik als eine Ursache von verschiedenen Alterungsprozessen im Blick. Bei der Epigenetik handelt es sich um Veränderungen an der Erbinformation und der Chromosomen, die nicht die Sequenz der DNA selbst verändern, aber ihre Aktivität beeinflussen können. Dies geschieht durch die Modifizierung von DNA und DNA-bindenden Proteinen, den sogenannten Histonen. An diesen Modifizierungen sind kleine Moleküle beteiligt, die aus dem Stoffwechsel der Zelle stammen und die DNA mehr oder weniger zugänglich machen können. Dies erlaubt nachfolgend die Bindung von Transkriptionsfaktoren, die die Gene an- oder abschalten. Durch diesen Prozess sind Stoffwechsel und Epigenetik eng miteinander verbunden und viele Stoffwechselprozesse selbst, aber auch die Ernährung jedes Einzelnen können so die Genexpression beeinflussen.
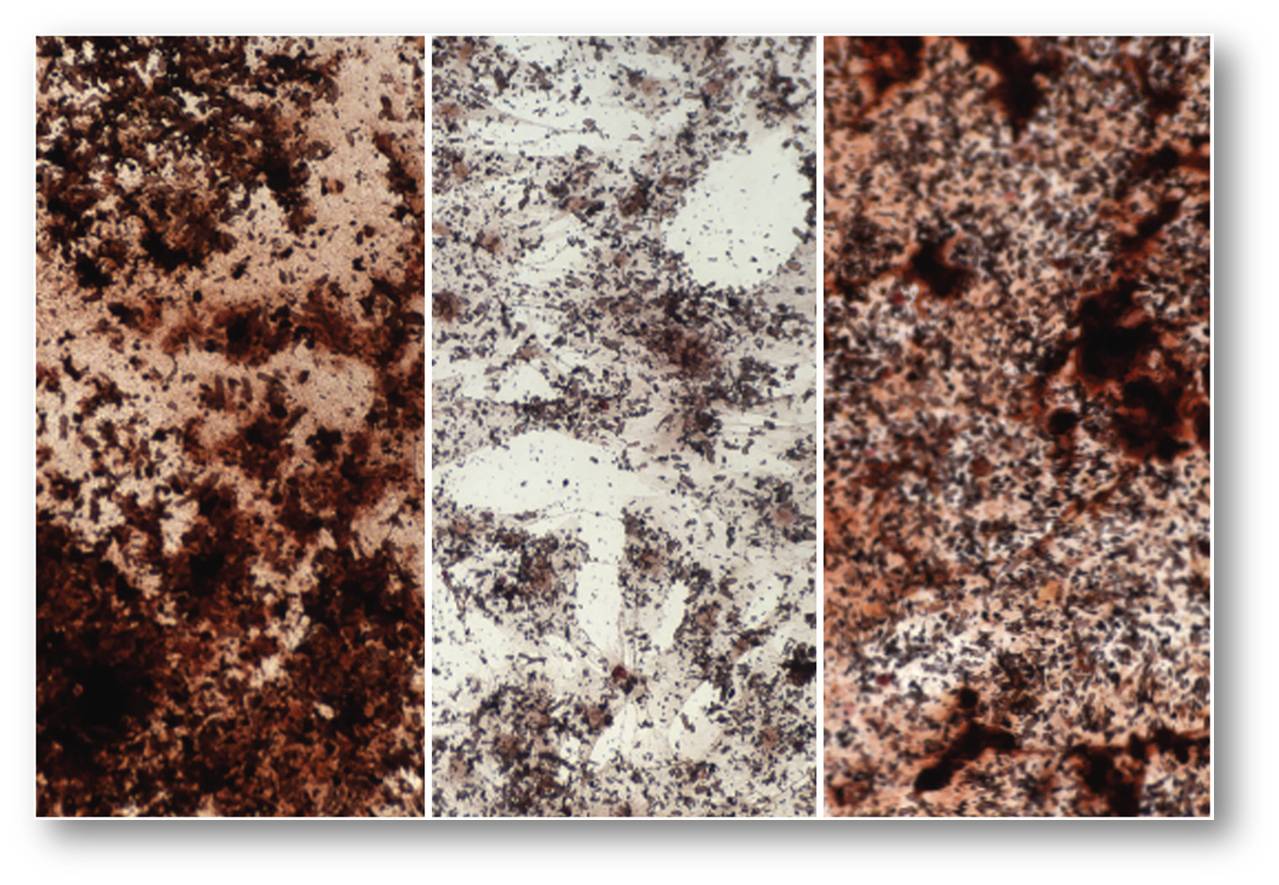
| Abbildung 1: Angefärbtes Kalzium (dunkelbraun) in Stammzellen im Knochenmark: Junge Stammzellen (links) produzieren mehr Material für den Knochenaufbau als alte Stammzellen (Mitte). In alten Stammzellen wiederum sammelt sich mehr Fettgewebe an. Durch Zugabe von Natriumazetat lassen sie sich aber wieder verjüngen (rechts). © Max-Planck-Institut für Biologie des Alterns/Pouikli 0 |
Da sich der Stoffwechsel mit zunehmendem Alter ändert, ist das Zusammenspiel zwischen Epigenetik und Stoffwechsel ein wichtiger Bestandteil des Alterns. Wir wollen und müssen diesen Aspekt des Alterns besser verstehen, um Ansätze zu entwickeln, die die Lebenszeit eines Menschen verlängern, und zwar um die Zeitspanne, in der er gesund leben kann (Abbildung 1). Eine besonders entscheidende Komponente des Stoffwechsels sind außerdem die Mitochondrien, kleine Organellen in unseren Zellen, die für die Gewinnung von Energie und die Herstellung vieler Stoffwechselprodukte sind. Eines dieser Produkte ist Acetyl-CoA, ein Molekül, das unter anderem in den Zellen benutzt wird, um Fette herzustellen und auch, wie erwähnt, um Histone, zu acetylieren – also kovalent zu modifizieren. Die DNA wird zugänglicher für Transkriptionsfaktoren, die dann Gene effizient anschalten können.
Wie hängen nun also Stoffwechsel, Epigenetik und dünne Knochen zusammen?
Um diese Frage zu klären, haben wir das Epigenom, also alle epigenetischen Veränderungen an der DNA einer Zelle, von mesenchymalen Stammzellen untersucht. Diese Stammzellen finden sich im Knochenmark und können verschiedene Zellarten wie Knorpel-, Knochen- und Fettzellen hervorbringen.
Die Rolle von Acetyl-CoA und der Mitochondrien
Wir wollten wissen, warum diese Stammzellen im Alter weniger Material für die Knochen produzieren und sich so immer mehr Fettgewebe im Knochenmark ansammelt. Deswegen haben wir das Epigenom von Stammzellen aus jungen und alten Mäusen verglichen. Im Alter ändert sich in der Tat das Epigenom sehr, vor allem wird die DNA weniger zugänglich. Diese Veränderungen betreffen häufig diejenigen Gene, die wichtig für die Herstellung von Knochen sind. Weiterhin konnten wir zeigen, dass im Alter weniger Acetylierungen vorliegen, und eine Erklärung dafür könnte sein, dass sich der Stoffwechsel derart verändert ist, dass Mitochondrien weniger Acetyl-CoA produzieren. Dieses aber ist nach unseren Untersuchungen nicht der Fall. Allerdings fanden wir heraus, dass Mitochondrien dieses Stoffwechselprodukt nur noch gering, verglichen mit jungen Mitochondrien, aus ihrem Inneren ausschleusen können. Schuld daran sind reduzierte Mengen eines Proteins (Slc25a1), das dafür verantwortlich ist, Acetyl-CoA von den Mitochondrien in das Cytoplasma zu transportieren [1].
Verjüngung des Epigenoms
Ein spannendes Ergebnis dieser Untersuchungen war, dass es ausgereicht hat, den älteren mesenchymalen Zellen über rekombinante Viren wieder mehr des Proteins Slc25a1 zu verabreichen. So wurde wieder mehr Acetyl-CoA ins Cytoplasma transportiert, die Histone wurden wieder acetyliert und es wurden wieder diejenigen Gene angeschaltet, die dafür sorgen, dass mehr Knochenzellen gebildet werden. Wir konnten sogar zeigen, dass allein schon die kurzfristige Zugabe eines anderen Vorläufers von Acetyl-CoA, nämlich Natriumacetat, zu isolierten Stammzellen ausreicht, das Epigenom zu verjüngen.
Um abschließend zu verstehen, ob die hier vorgestellten Veränderungen im Epigenom auch beim Menschen die Ursache für das im Alter erhöhte Risiko für Knochenbrüche oder Osteoporose sein könnte, untersuchten wir menschliche mesenchymale Stammzellen, die wir nach einer Hüftoperation von Patienten erhielten. Die Zellen von älteren Patienten, die auch an Osteoporose litten, zeigten tatsächlich dieselben epigenetischen Veränderungen, wie sie bereits zuvor bei den Mäusen beobachtet wurden. Dieses zeigt, dass auch im Menschen die Ursachen von dünnen Knochen im Alter wahrscheinlich im Epigenom zu suchen sind.
Neben unserer Studie wurden in den letzten Jahren auch andere Beispiele vorgestellt, die aufgezeigt haben, wie eng Stoffwechsel und Epigenom miteinander verflochten sind. Diese Verbindung ist scheinbar nicht nur ein zentraler Bestandteil des Alterns, sondern spielt auch bei anderen biologischen Prozessen eine entscheidende Rolle. Als Beispiel sei die Embryonalentwicklung zu nennen, wo Änderungen im Stoffwechsel und nachfolgend im Epigenom eng miteinander gekoppelt sind. Auch Erkrankungen, wie zum Beispiel die Entstehung von Tumoren, bei denen sich sowohl Stoffwechsel als auch das Epigenom sehr stark verändern, müssen hier erwähnt werden. In den nächsten Jahren wird es von großer Bedeutung sein, das Zusammenspiel zwischen Stoffwechsel, Epigenetik und Genexpression noch besser zu verstehen, um darauf aufbauend Therapieansätze zu entwickeln. Vielleicht wird es dann in Zukunft auch möglich sein, alte Stammzellen wieder verjüngen zu können und sie im Rahmen einer Stammzelltherapie einzusetzen.
--------------------------------------
[1] Pouikli, A.; Parekh, S.; Maleszewska, M.; Nikopoulou, C.; Baghdadi, M.; Tripodi, I.; Folz-Donahue, K.; Hinze, Y.; Mesaros, A.; Hoey, D.; Giavalisco, P.; Dowell, R.; Partridge, L.; Tessarz, P. Chromatin remodeling due to degradation of citrate carrier impairs osteogenesis of aged mesenchymal stem cells Nature Aging 1, 810–825 (2021)
*Der Forschungsbericht mit dem Titel „Verjüngungskur für alternde Stammzellen im Knochenmark" (https://www.mpg.de/18101170/age_jb_2021?c=155461) stammt aus dem Jahrbuch 2021 der Max-Planck-Gesellschaft, das im Sommer 2022 erschienen ist; mit Ausnahme des marginal veränderten Titels wurde der Bericht unverändert in den Blog übernommen. Die MPG-Pressestelle hat freundlicherweise zugestimmt, dass wir von MPG-Forschern verfasste Artikel in den ScienceBlog stellen können.
Weiterführende Links
Max-Planck-Institut für Biologie des Alterns: https://www.mpg.de/155461/biologie-des-alterns
Peter Tessarz: Epigenetics and Ageing: Fountain of youth for ageing stem cells in bone marrow (deutsche Untertitel). Video 3:09 min. (13.September 2021) https://www.youtube.com/watch?v=FbwcbFoNInI
Max-Planck-Cinema: Epigenetik - Änderungen jenseits des genetischen Codes.
Peter Spork, Newsletter Epigenetik: https://www.peter-spork.de/86-0-Newsletter-Epigenetik.html
Epigenetik im ScienceBlog:
- Christina Beck, 15.09.2022: Epigenetik - Wie die Umsetzung unserer Erbinformation gesteuert wird
- Gottfried Schatz, 22.08.2014: Jenseits der Gene — Wie uns der Informationsreichtum der Erbsubstanz Freiheit schenkt
- Norbert Bischofberger, 24.05.2018: Auf dem Weg zu einer Medizin der Zukunft
- Peter Schuster, 12.03.2020: Molekularbiologie im 21. Jahrhundert
- Printer-friendly version
- Log in to post comments