Do, 02.01.2020 — Arturo Zychlinsky

![]() Ein Organismus wird tagtäglich mit einer Vielzahl von Krankheitserregern konfrontiert. Das Immunsystem hat daher im Laufe der Evolution viele ausgeklügelte Abwehrmechanismen entwickelt. Das Team um Prof. Arturo Zychlinsky (Direktor am Max-Planck-Institut für Infektionsbiologie, Berlin) hat 2004 einen bis dahin unbekannten Mechanismus beschrieben: Neutrophile Granulozyten als Zellen des Immunsystems können schädliche Mikroorganismen in Netzen fangen. Interessanterweise sind diese Netze im Wesentlichen nicht nur aus den gleichen Bestandteilen wie die Erbsubstanz aufgebaut, bei der Netzbildung laufen auch Schritte ab, die sonst nur bei der Zellteilung stattfinden.
Ein Organismus wird tagtäglich mit einer Vielzahl von Krankheitserregern konfrontiert. Das Immunsystem hat daher im Laufe der Evolution viele ausgeklügelte Abwehrmechanismen entwickelt. Das Team um Prof. Arturo Zychlinsky (Direktor am Max-Planck-Institut für Infektionsbiologie, Berlin) hat 2004 einen bis dahin unbekannten Mechanismus beschrieben: Neutrophile Granulozyten als Zellen des Immunsystems können schädliche Mikroorganismen in Netzen fangen. Interessanterweise sind diese Netze im Wesentlichen nicht nur aus den gleichen Bestandteilen wie die Erbsubstanz aufgebaut, bei der Netzbildung laufen auch Schritte ab, die sonst nur bei der Zellteilung stattfinden.
Krankheitserreger gehen ins Netz
Neutrophile Granulozyten, kurz Neutrophile genannt, sind die am häufigsten vorkommenden weißen Blutzellen im menschlichen Organismus. Sie gehören zu denjenigen Zellen, die als erstes vor Ort sind, um eingedrungene Pathogene unschädlich zu machen. Sie haben dazu hauptsächlich drei Strategien entwickelt.
Sie können Pathogene phagozytieren und in ihrem Zellinneren verdauen.
Sie können aber auch antimikrobielle Proteine aus den Granula in den Zellzwischenraum ausscheiden und den Pathogenen damit eine unwirtliche Umgebung bereiten.
Ein in unserem Labor vor rund 15 Jahren im Detail beschriebenes Phänomen ist die Bildung von Neutrophil Extracellular Traps, kurz NETs.
NETs sind netzartige Strukturen, die Neutrophile bei Kontakt mit Pathogenen auswerfen. Dabei sterben die Neutrophilen einen speziellen Zelltod, NETosis genannt. Bemerkenswert ist der Aufbau der Netze. Sie werden aus der DNA der Neutrophilen gebildet und sind wie mit Perlen über und über mit Proteinen aus den Granula und mit Histonen besetzt. Histone sind Proteine aus dem Zellkern, die dafür sorgen, dass die DNA in Chromatin aufgewickelt vorliegt. Zusätzlich können Histone Bakterien effizient abtöten. In den NETs werden die eingefangenen Pathogene unter anderem durch elektrische Ladungsunterschiede festgehalten und nachfolgend von Granulaproteinen und Histonen abgetötet.
Viele Wege führen zur Bildung von NETs
Die genauen molekularen Mechanismen der NETosis und NET-Bildung sind noch nicht verstanden. Dies liegt vor allem daran, dass Neutrophile experimentell schwer zu untersuchen sind. Einerseits sind diese Zellen leicht zu aktivieren, andererseits haben sie außerhalb des Körpers nur eine Lebensdauer von wenigen Stunden.
Unserem Labor gelang es, standardisierte experimentelle Bedingungen für vergleichbare und quantifizierbare Untersuchungen zu erzeugen. Unter diesen Bedingungen stimulierten wir Neutrophile mit zwei Pathogenen - dem Hefepilz Candida albicans und Streptokokken der Gruppe B - sowie mit Ionophoren, also Substanzen, die den Ionenhaushalt in den Neutrophilen beeinflussen [1]. Alle diese Stimuli induzierten die Bildung von NETs, die vergleichbare Eigenschaften zeigten (Abbildung 1).
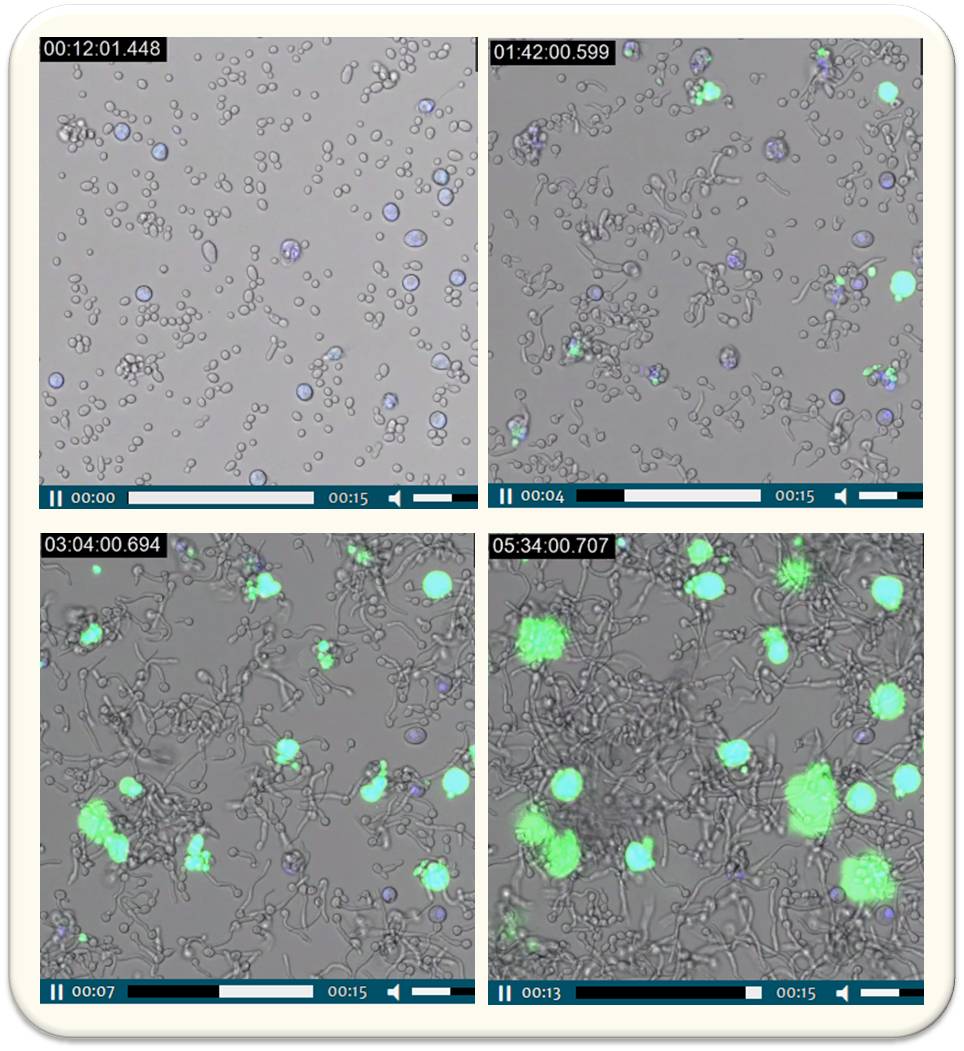 Abbildung 1. Candida albicans induzierte NETosis in humanen primären Neutrophilen. Die Neutrophilen wurden mit dem blauen Fluoreszenzfarbstoff Draq5, der Zellmembranen passieren kann, und dem grünen Fluoreszenzfarbstoff Sytox Green, der Zellmembranen nicht passieren kann, gefärbt. Das Auftreten der grünen Fluoreszenz zeigt das Auftreten von NETosis an. (Die Bilder sind Screenshots aus einem kurzen Video, das im Original https://www.mpg.de/13489596/mpiib-berlin_jb_2018?c=15261 0 gesehen werden kann; Anm. Redn)
Abbildung 1. Candida albicans induzierte NETosis in humanen primären Neutrophilen. Die Neutrophilen wurden mit dem blauen Fluoreszenzfarbstoff Draq5, der Zellmembranen passieren kann, und dem grünen Fluoreszenzfarbstoff Sytox Green, der Zellmembranen nicht passieren kann, gefärbt. Das Auftreten der grünen Fluoreszenz zeigt das Auftreten von NETosis an. (Die Bilder sind Screenshots aus einem kurzen Video, das im Original https://www.mpg.de/13489596/mpiib-berlin_jb_2018?c=15261 0 gesehen werden kann; Anm. Redn)
Setzten wir Substanzen ein, die mögliche Signalwege während der NETosis blockieren könnten, zeigten sich Unterschiede. Für die NET-Bildung nach Stimulierung mit den Pathogenen etwa spielen reaktive Sauerstoffspezies, sogenannte Sauerstoffradikale, eine Rolle, nach der Stimulierung mit Ionophoren dagegen nicht. Auf der Basis dieser und weiterer Ergebnisse konnten wir einen Atlas von Signalwegen erstellen, der zeigt, dass je nach Stimulus ein anderer Signalweg für die Bildung von NETs eingeschlagen wird.
Zellteilung mit Abzweigung in Richtung NETs?
DNA und Histone aus dem Zellkern und Proteine aus den Granula müssen sich vor der NET-Bildung im Zellplasma mischen können. Dies setzt den Abbau der Kern- und Granulamembranen voraus. Die Kernmembran wiederum wird auch während der Zellteilung, der Mitose, aufgelöst. Daher fragten wir uns, ob NET-Bildung und Mitose eventuell Parallelen aufweisen.
Zunächst untersuchten wir stimulierte Neutrophile auf Merkmale, die für bestimmte Phasen der Mitose typisch sind. So konnten wir zeigen, dass Lamine, spezielle Proteine der Kernmembran, in den Neutrophilen phosphoryliert vorliegen. Dadurch wird die Festigkeit der Kernmembran aufgehoben und sie kann sich auflösen. Die Replikation der DNA, typisch für die Mitose, konnten wir dagegen nicht nachweisen.
Besonders interessant war die Beobachtung, dass sich in stimulierten Neutrophilen Zentrosomen bilden und auseinanderdriften (Abbildung 2). Zentrosomen sind Strukturen aus Mikrotubuli, die während der Mitose an die gegenüberliegenden Pole der sich teilenden Zelle wandern. An den Zentrosomen ist die mitotische Spindel aufgehängt, die die Chromosomen auseinanderzieht. In den untersuchten Neutrophilen konnten wir allerdings keine mitotische Spindel beobachten.
 Abbildung 2. Verdoppelung und Trennung der Zentrosomen während der NET-Bildung. In stimulierten Neutrophilen wurden Zentrosomen mit Hilfe eines anti-Tubulin-Antikörpers rot gefärbt. Die DNA ist mit einem blauen Farbstoff markiert. Drei Stunden nach der Stimulation (rechtes Bild) werden NETs beobachtet.© Max-Planck-Institut für Infektionsbiologie/Amulic; Brinkmann
Abbildung 2. Verdoppelung und Trennung der Zentrosomen während der NET-Bildung. In stimulierten Neutrophilen wurden Zentrosomen mit Hilfe eines anti-Tubulin-Antikörpers rot gefärbt. Die DNA ist mit einem blauen Farbstoff markiert. Drei Stunden nach der Stimulation (rechtes Bild) werden NETs beobachtet.© Max-Planck-Institut für Infektionsbiologie/Amulic; Brinkmann
Der Zellzyklus in sich teilenden Zellen durchläuft mehrere sogenannte Checkpoints. DNA-Schäden, Zellgröße, Zelldichte und viele andere Faktoren werden an den Checkpoints überwacht und können zur Unterbrechung der Zellteilung oder zum programmierten Zelltod, der sogenannten Apoptose, führen. Spezialisierte Zellzyklusproteine wie Zykline und Zyklin-abhängige Kinasen steuern diesen Prozess. In unseren Experimenten bewirkte die Stimulierung der Neutrophilen eine Aktivierung von CDK4/6-Kinasen, die in ruhenden Zellen zum Eintritt in die Mitose führen. Es bleibt offen, wie diese Zyklin-abhängigen Kinasen in Neutrophilen einen Teil der Mitose-Maschinerie anwerfen können.
Löcher im Immunsystem
In den letzten Jahren wurden NETs immer häufiger mit autoinflammatorischen und Autoimmunerkrankungen in Verbindung gebracht. Bei der Autoimmunkrankheit Lupus beispielsweise werden gegen die sich in den NETs befindende DNA Antikörper gebildet, die zu Nierenschäden führen können.
Lupus scheint darüber hinaus mit einer überschießenden NET-Produktion verbunden zu sein. Für uns war es daher von Interesse herauszufinden, wie beziehungsweise mit welchen Substanzen die NET-Bildung inhibiert werden kann. In Kooperation mit dem Lead Discovery Center (LDC), einer Ausgründung der Max-Planck-Gesellschaft, starteten wir ein großangelegtes Screening; annähernd 200.000 Substanzen wurden dabei auf ihre Fähigkeit getestet, NETs zu inhibieren. Für eine Substanz gelang es, ihren Wirkungsmechanismus näher zu untersuchen und ihr Target, also ihren Wirkort, zu identifizieren: Gasdermin D. Diese Entdeckung war besonders interessant, da es sich bei Gasdermin D um ein porenbildendes Protein handelt. Unsere Experimente mit dem neu identifizierten Gasdermin D-Inhibitor lassen vermuten, dass Gasdermin D dazu beiträgt, die Neutrophilen-Zellmembran derart z Max-Planck-Institut für Infektionsbiologie, Berlin u perforieren, dass NETs durch die entstandenen Löcher ausgeworfen werden können.
Dies bietet neue Ansätze für die klinische Forschung an Krankheiten, die mit einer Überproduktion von NETs einhergehen.
* Der vorliegende Artikel ist im Jahrbuch 2018 der Max-Planck-Gesellschaft unter identem Titel "Neutrophile: Zwischen Zellteilung und Zelltod" https://www.mpg.de/13489596/mpiib-berlin_jb_2018?c=15261 0 erschienen und wurde mit freundlicher Zustimmung der MPG-Pressestelle ScienceBlog.at zur Verfügung gestellt. Der Artikel wurde unverändert übernommen, allerdings ohne Literaturzitate - diese können im Original nachgesehen werden.
Weiterführende Links
Max-Planck-Institut für Infektionsbiologie, Berlin
ESDR2019 Celgene Lecture: Arturo Zychlinsky "NETs in health and disease" Video 23:32 min.
- Printer-friendly version
- Log in to post comments
