Ein Comeback der Phagentherapie?
Ein Comeback der Phagentherapie?Do, 29.08.2019 — Karin Moelling

![]() Viren, die spezifisch Bakterien befallen, sogenannte Bakteriophagen (kurz Phagen), wurden bereits vor einem Jahrhundert entdeckt und therapeutisch gegen bakterielle Infektionen eingesetzt. Als Antibiotika ihren Siegeszug antraten, gerieten Phagen aber in den meisten Ländern in Vergessenheit. Die Entstehung von Antibiotika-resistenten Bakterien und der Mangel an neuen wirksamen Substanzen hat nun das Interesse an einer Phagentherapie wieder aufleben lassen. Was Phagen sind und wie sie funktionieren hat die renommierte Virologin Karin Moelling (em. Prof. für Virologie der Universität Zürich und Gruppenleiterin am Max-Planck-Institut für molekulare Genetik) in einem vorangegangenen Artikel dargestellt [1]. Nun schreibt sie über die therapeutische Anwendung von Phagen und nennt vielversprechende Beispiele.
Viren, die spezifisch Bakterien befallen, sogenannte Bakteriophagen (kurz Phagen), wurden bereits vor einem Jahrhundert entdeckt und therapeutisch gegen bakterielle Infektionen eingesetzt. Als Antibiotika ihren Siegeszug antraten, gerieten Phagen aber in den meisten Ländern in Vergessenheit. Die Entstehung von Antibiotika-resistenten Bakterien und der Mangel an neuen wirksamen Substanzen hat nun das Interesse an einer Phagentherapie wieder aufleben lassen. Was Phagen sind und wie sie funktionieren hat die renommierte Virologin Karin Moelling (em. Prof. für Virologie der Universität Zürich und Gruppenleiterin am Max-Planck-Institut für molekulare Genetik) in einem vorangegangenen Artikel dargestellt [1]. Nun schreibt sie über die therapeutische Anwendung von Phagen und nennt vielversprechende Beispiele.
Von Bakterien, gegen die kein Antibiotikum mehr hilft…
Die rasante Resistenzentwicklung gegen das Arsenal vorhandener Antibiotika stellt eine der größten weltweiten Bedrohungen für Gesundheit und übliche medizinische Praktiken (wie Operationen, Tumorbehandlungen) dar. Das Problem wird noch dadurch verschärft, dass antibakteriell wirksame neue Substanzen - zumindest im Laufe des nächsten Jahrzehnts - nicht in Sicht sind. Aktuell geht die WHO davon aus, dass weltweit mindestens 700 000 Personen jährlich an Infektionen mit resistenten Keimen versterben (im worst-case Szenario kann diese Zahl im Jahr 2050 auf 10 Millionen anwachsen) [2], in der Europäischen Union schätzt man jährlich auf 33 000 derartige Todesfälle [3], allein in Berlin ist es jede Woche ein Opfer.
Auf der immer dringlicher werdenden Suche nach Alternativen zur Behandlung bakterieller Infektionen erinnern sich Forscher nun wieder an eine mögliche Anwendung von Phagen, die sogenannte Phagentherapie. Abbildung 1.
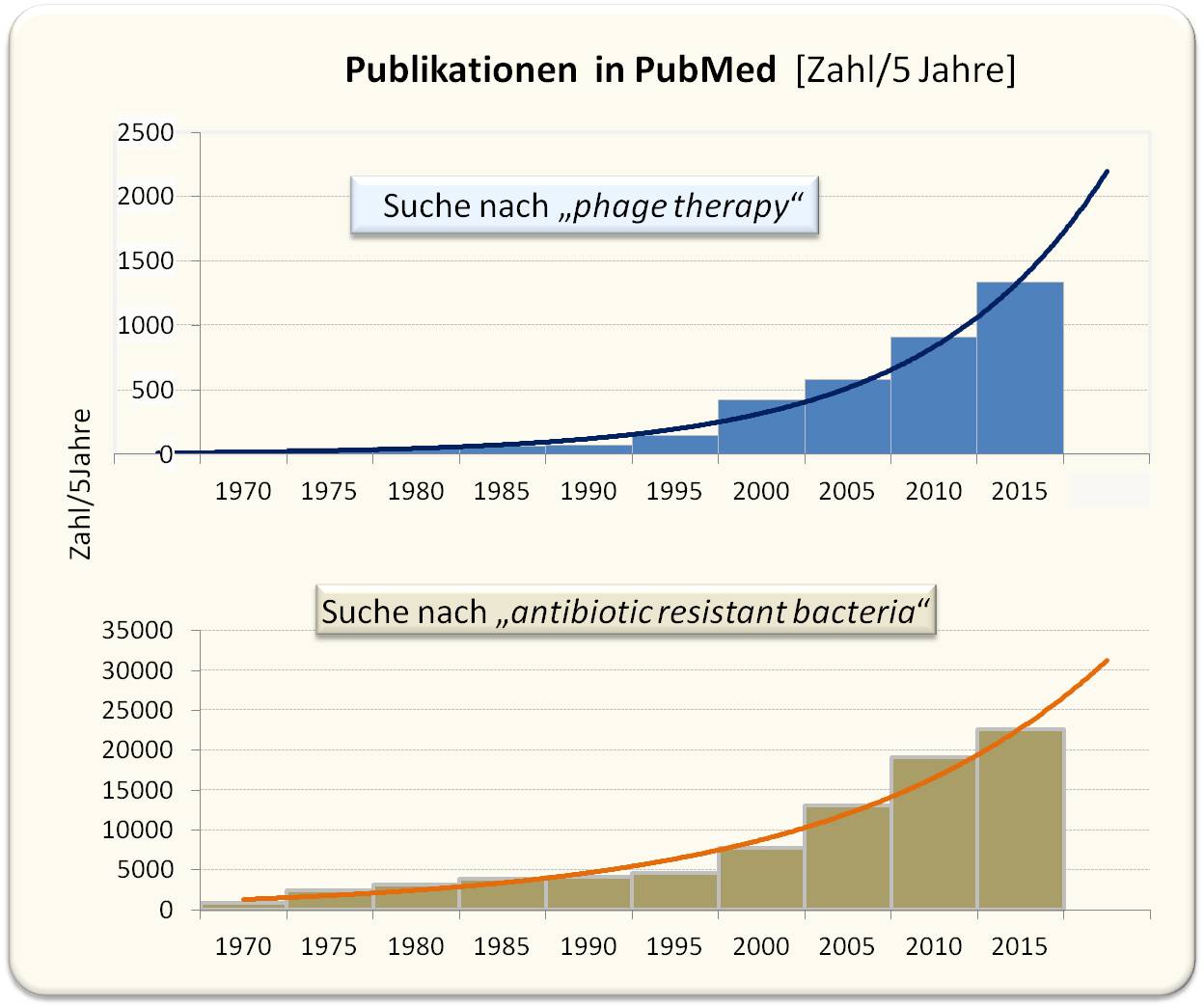 Abbildung 1. Publikationen in Pubmed (der größten (bio)medizinischen Datenbank): Ab dem Jahr 2000 kommt es zu einem exponentiellen Anstieg von Arbeiten über Antibiotika-resistente Bakterien und ebenso über Phagentherapie. (Zahl der Publikationen über jeweils 5 Jahre summiert; Grafik mit exponentiellen Trendlinien in Microsoft Excel erstellt).
Abbildung 1. Publikationen in Pubmed (der größten (bio)medizinischen Datenbank): Ab dem Jahr 2000 kommt es zu einem exponentiellen Anstieg von Arbeiten über Antibiotika-resistente Bakterien und ebenso über Phagentherapie. (Zahl der Publikationen über jeweils 5 Jahre summiert; Grafik mit exponentiellen Trendlinien in Microsoft Excel erstellt).
…zur Phagentherapie…
Wie schon in [1] geschildert, ist die Phagentherapie kein neues Konzept. Vor etwas mehr als hundert Jahren hat Félix d’Hérelle (1873–1949) am Institut Pasteur aus Stuhlproben von an bakterieller Ruhr erkrankten Patienten "unsichtbare Mikroben" isoliert, welche er - da sie gezüchtete Rasen von Ruhr-Bakterien zerstörten - als Bakteriophagen (Bakterienfresser) bezeichnete. (Wie Phagen dabei in hochspezifischer Weise Bakterien attackieren und zerstören, ist in [1] beschrieben.) d’Hérelle hatte auch gleich das therapeutische Potential seiner Entdeckung erkannt: die Anwendung dieser Bakteriophagen bei bakteriellen Infektionen. "Ultramikroskopische, nicht-pathogene Viren" im Filtrat von Bakterienkulturen hatte einige Jahre zuvor auch schon der britische Bakteriologe Frederick Twort entdeckt; der Ausbruch des Weltkriegs stoppte seine Untersuchungen, die er nach Kriegsende nicht fortsetzte.
Aber bereits lange zuvor wurde die - wahrscheinlich auf Phagen beruhende - heilsame Wirkung von menschlichem oder tierischem Kot bei bakteriellen Infektionen von Mensch und Tier erfolgreich angewandt (Kot enthält immerhin bis zu 10 Milliarden Phagen pro Gramm Trockengewicht): Im China des 4. Jahrhunderts verschrieben Mediziner aufgeschlämmten menschlichen Stuhl ("Gelbe Suppe") bei Durchfall und Nahrungsmittelvergiftungen, Beduinen wandten Kamelkot an - Praktiken, die bei uns bis jetzt ins Reich der Märchen verwiesen worden sind.
Dass Inder trotz der Verschmutzungen durch Fäkalabwässer und treibende Leichenreste seit Jahrhunderten weitgehend unbeschadet in den heiligen Flüssen Ganges und Yamuna rituell baden und das Flusswasser trinken, hat den englischen Bakteriologen Ernest Hankin sehr erstaunt. Im Jahr 1896 untersuchte er Wasserproben, nachdem er sie durch ein Porzellanfilter filtriert hatte, das für Teilchen ab der Größe von Bakterien undurchlässig war. Im Filtrat stellte er hohe Aktivität gegen Cholerabakterien fest, die offensichtlich biologischer Natur war, da sie beim Erhitzen verloren ging - diese Aktivität dürfte wahrscheinlich auf die damals noch unbekannten Phagen zurückzuführen gewesen sein. Abbildung 2.
 Abbildung 2. Baden im heiligen Fluss Ganges an einem der Ghats in Varanasi. Links und rechts unten: Der englische Bakteriologe Ernest Hankin wies 1896 im Flusswasser hohe antibakterielle Aktivität gegen Cholerakeime nach, die beim Erhitzen verschwand. Rechts: Während Festen wie Kumbh Mela baden Millionen Inder im Ganges ohne, dass es zum Ausbruch von Epidemien kommt. (Bild: Thonas Hoffmann, 2018; Flickr cc- by- nc-sa)
Abbildung 2. Baden im heiligen Fluss Ganges an einem der Ghats in Varanasi. Links und rechts unten: Der englische Bakteriologe Ernest Hankin wies 1896 im Flusswasser hohe antibakterielle Aktivität gegen Cholerakeime nach, die beim Erhitzen verschwand. Rechts: Während Festen wie Kumbh Mela baden Millionen Inder im Ganges ohne, dass es zum Ausbruch von Epidemien kommt. (Bild: Thonas Hoffmann, 2018; Flickr cc- by- nc-sa)
…und ihre Entwicklung bis ins Zeitalter der Antibiotika
Nach einigen Tierversuchen wurden Phagen bald am Menschen angewandt. 1921 wurden in einem Pariser Kinderspital die an Bakterienruhr erkrankten jungen Patienten innerhalb eines Tages geheilt. d’Hérelle selbst reiste unentwegt an Orte, wo Infektionen - insbesondere Cholera und Pest - grassierten (nach Südamerika, Mexiko, Indien, in verschiedene afrikanische Staaten und auch nach Russland) und behandelte die Patienten mit einem Gemisch von Phagen als "cocktails", die er passgenau auf die zu behandelnden Infektionen abstimmte. Überzeugt davon, dass Phagen in spezifischer Weise Bakterien aber nicht höhere Lebewesen befallen und für diese daher harmlos sind, schluckte d’Hérelle auch selbst seine Cocktails ohne Nebenwirkungen zu verspüren. In Tiflis (Georgien) gründete er 1936 mit Georgi Eliava das Georgi Eliava Institut für Phagenforschung, das heute noch existiert, Phagen herstellt und nun zu einer Zuflucht für Patienten aus aller Welt wird, die an Antibiotika-resistenten Infektionen leiden. Zuvor war das Militär Hauptabnehmer für die Phagenpräparate des Eliava-Instituts. Man verzeichnete bereits 1939 - während des Finnisch-Russischen Krieges - große Erfolge: 6 000 Soldaten mit infizierten Wunden erhielten Phagencocktails in die offenen Wunden geträufelt; 80 % wurden gesund und Amputationen wurden ihnen erspart.
Bis in die 1940er Jahre wurden Phagen-Präparate in Europa und Amerika angewandt; Hersteller waren u.a. Pharmaunternehmen wie Behring, Eli Lilly, Abbott, Parke-Davis und Squibb. Für den einfacheren Versand wurden Präparate in Form von Pulver oder Pillen entwickelt und auch noch im 2. Weltkrieg in Feldlazaretten genutzt.
Als aber in den 1940er Jahren mit kommerziell erhältlichem Penicillin die Ära der Antibiotika anbrach, welche ein breites Spektrum von Bakterien auch ohne passgenaue Abstimmung töteten, geriet die Phagentherapie zumindest in den westlichen Staaten in Vergessenheit. Da man nun Phagentherapie als entbehrlich ansah, wurden in den 1980er Jahren schließlich die Bestände an Phagenkollektionen vielerorts, auch am Pasteur-Institut und in Lyon vernichtet. In Ländern hinter dem Eisernen Vorhang - vor allem Russland, Georgien und Polen -, in denen Antibiotika lange Zeit nicht erhältlich waren, blieb die Phagentherapie weiter bestehen und wird auch heute routinemäßig durchgeführt.
Ein Comeback der Phagen
Über die therapeutische Anwendung hinaus haben Phagen bereits in einigen Sparten Anwendung gefunden.
…für nicht-therapeutische Anwendungen
2006 in den US für die Konservierung von Lebensmitteln zugelassen, werden Phagen seitdem in zahlreichen Staaten und auch in EU-Ländern eingesetzt. Es handelt sich hier vor allem um Phagen, die spezifisch gegen gefährliche Listerienstämme gerichtet sind, wie sie u.a. in Räucherlachs, Fertigsalaten, Rohmilchprodukten, etc. vorkommen können; diese Lebensmittel werden nun vor dem Verpacken einem Sprühnebel aus Phagen ausgesetzt oder mit diesen eingestrichen. Da Phagen - wie erwähnt - für höhere Organismen harmlos sind, brauchen sie auf den Verpackungen nicht deklariert werden.
In der Landwirtschaft werden Phagen u.a. als biologische Pflanzenschutzmittel im Obst-und Weinbau eingesetzt. Mit Phagen kann auch die bakterielle Fäulnis von Kartoffeln bekämpft und der Ernteertrag so um ein Mehrfaches gesteigert werden.
Weitere nicht-therapeutische Anwendungen finden Phagen als schnelle, hochsensitive Diagnostika für Bakterienstämme oder als biologische Desinfektionsmittel z.B. von mit Listerien oder Salmonellen verseuchten Räumen.
…für therapeutische Anwendungen…
In den vergangenen Jahren gab es viele Beispiele für Heilungen von bakteriellen Infektionen, insbesondere von solchen mit multi-resistenten Keimen; das Spektrum reicht von schwerem Brechdurchfall, Harnwegsinfekten über Entzündungen des Nasen-Rachenraums bis zu hin Wundinfektionen, "offenen" Beinen, ulzerierenden Zehen von Diabetikern, offenen Frakturen, etc.
Das Problem bei diesen Beispielen ist allerdings, dass es sich dabei häufig um Fallstudien handelt, die nicht den behördlichen Richtlinien von klinischen Studien entsprechen, welche randomisiert, Placebo-kontrolliert als Doppelblind-Studien erfolgen sollen.
…und einige Beispiele
Zu den erfolgreichen Fallstudien aus den letzten Jahren zählt wohl der - auch durch YouTube-Videos populär gewordene - Fall des kalifornischen Professors Tom Patterson. Als dieser 2015 mit seiner Frau Ägypten bereiste, zog er sich eine Infektion mit einem multiresistenten Stamm von Acinetobacter baumannii zu, der eine lebensbedrohende Pankreatitis und Diabetes auslöste. Patterson wurde an die heimatliche Universitätsklinik San Diego gebracht, fiel ins Koma und war von den Ärzten bereits aufgegeben, nicht aber von seiner Frau Steffanie Strathdee. Selbst Epidemiologin setzte sie Kollegen, Ärzte und Gesundheitsbehörden in Bewegung: gegen den infektiösen Keim wurden passende Phagen gefunden, die amerikanische Zulassungsbehörde FDA gab 2016 für den Notfall eine Sondererlaubnis für eine "Investigative New Drug" (IND) Application. Nach nur drei intravenös verabreichten Dosen des Phagencocktails erholte sich der Patient sehr rasch und ist nun gesund. In den US war dies der erste Fall der als experimentell eingestuften Phagentherapie; seitdem wurden in San Diego weitere Patienten damit erfolgreich behandelt (Center for Innovative Phage Applications and Therapeutics (IPATH)).
Bei mehr als 420 Millionen Diabetikern weltweit (https://www.who.int/news-room/fact-sheets/detail/diabetes) wird ein sehr hohes Potential der Phagentherapie in der Behandlung des diabetischen Fusses/der Zehe gesehen. Häufig mit multiresistenten Keimen infiziert entstehen hier tiefe, nicht heilende Wunden und Amputationen bleiben in Hunderttausenden Fällen dann der einzige Ausweg. Zu dieser Indikation läuft seit 2013 eine systematische Multizentren-Studie, Phagopied, die Phagentherapie versus Standardbehandlung untersucht. Elizabeth Kutter (Evergreen Lab, Washington), eine prominente Verfechterin der Phagentherapie, hat vor kurzem die erfolgreiche Behandlung von einigen Patienten mit Phagencocktails gegen Staphylococcus aureus berichtet; Fotos zeigten anfangs bereits brandige Zehen und bei allen Patienten zugeheilte Wunden nach 2 Monaten; Amputationen erübrigten sich.
Bereits vor 11 Jahren suchte eine Patientin bei uns am Züricher Universitätsspital Hilfe; sie litt an chronischem Durchfall verursacht durch eine Infektion mit Clostridium difficile - offensichtlich als Folge einer mit Antibiotika behandelten Kieferentzündung. Gegen den vehementen Protest der Kliniker setzte die Patientin durch eine Stuhltransplantation zu erhalten: nach einem Einlauf mit dem klaren Überstand einer aufgeschlämmten Stuhlprobe war sie innerhalb weniger Tage geheilt. Prof Karin Moelling, ehemalige Virologin der Universität Zürich, hat mit Kollegen aus Zürich und Berlin haben in der Folge die Darmflora - Mikrobiom und Virom - der Patientin über acht Jahre regelmäßig untersucht und mit der des Donors verglichen: während die Phagenpopulation bereits innerhalb kürzester Zeit der Donorpopulation ähnlich wurde, war dies bei der Bakterienpopulation erst nach vier Jahren der Fall. Tatsächlich sollte vielleicht die Stuhltransplantation eher als Phagentherapie denn als Bakterientherapie betrachtet werden, da Phagen ja die um Größenordnungen überwiegende Population ausmachen. Nach einer Reihe erfolgreicher Fallstudien erteilte übrigens die US-Gesundheitsbehörde FDA 2013 die Zulassung der Stuhltransplantation für die Indikation der Clostridium Infektion. Innerhalb weniger Jahre hat diese Methode in der Ärzteschaft nun Akzeptanz gefunden und gilt auch bei anderen Infektionskrankheiten als aussichtsreich.
Im ehemaligen Ostblockland Polen haben sich Ärzte am Ludwig-Hirszfeld-Institut in Breslau auf die Phagentherapie spezialisiert. Eigenen Angaben zufolge wurden seit 1980 bereits mehr als 1500 mit antibiotikaresistenten Keimen infizierte Patienten meist erfolgreich mit Bakteriophagen behandelt.
Was es zur Phagentherapie braucht
In erster Linie fehlt es an verfügbaren Phagen. Weltweit gibt es zu wenige Sammlungen von spezifisch gegen pathogene Bakterienstämme wirksamen Phagen, welche für Therapiezwecke rasch vermehrt und geliefert werden können. Eine aktuelle Liste (https://phage.directory/) nennt 22 solcher Quellen - Phagenbanken, Biotech-Startups und nicht-kommerzielle Organisationen -, darunter u.a. das Leibniz Institut ("Deutsche Sammlung von Mikroorganismen und Zellkulturen" DSMZ; Braunschweig), die holländische "Fagenbank" und das" Eliava-Institut".
Verfügbare hochgereinigte und gut charakterisierte Phagen
Phagen gibt es überall, wo es Bakterien gibt: Jeder natürliche Bereich, in dem (pathogene) Bakterien vorkommen, enthält wahrscheinlich auch Phagen, die für diese Keime spezifisch sind und zu deren Lyse führen. Aus solchen Proben können Phagen relativ einfach isoliert, charakterisiert und getestet werden. Es sind dies Standardverfahren in mehreren aufeinanderfolgenden Schritten (Abbildung 3):
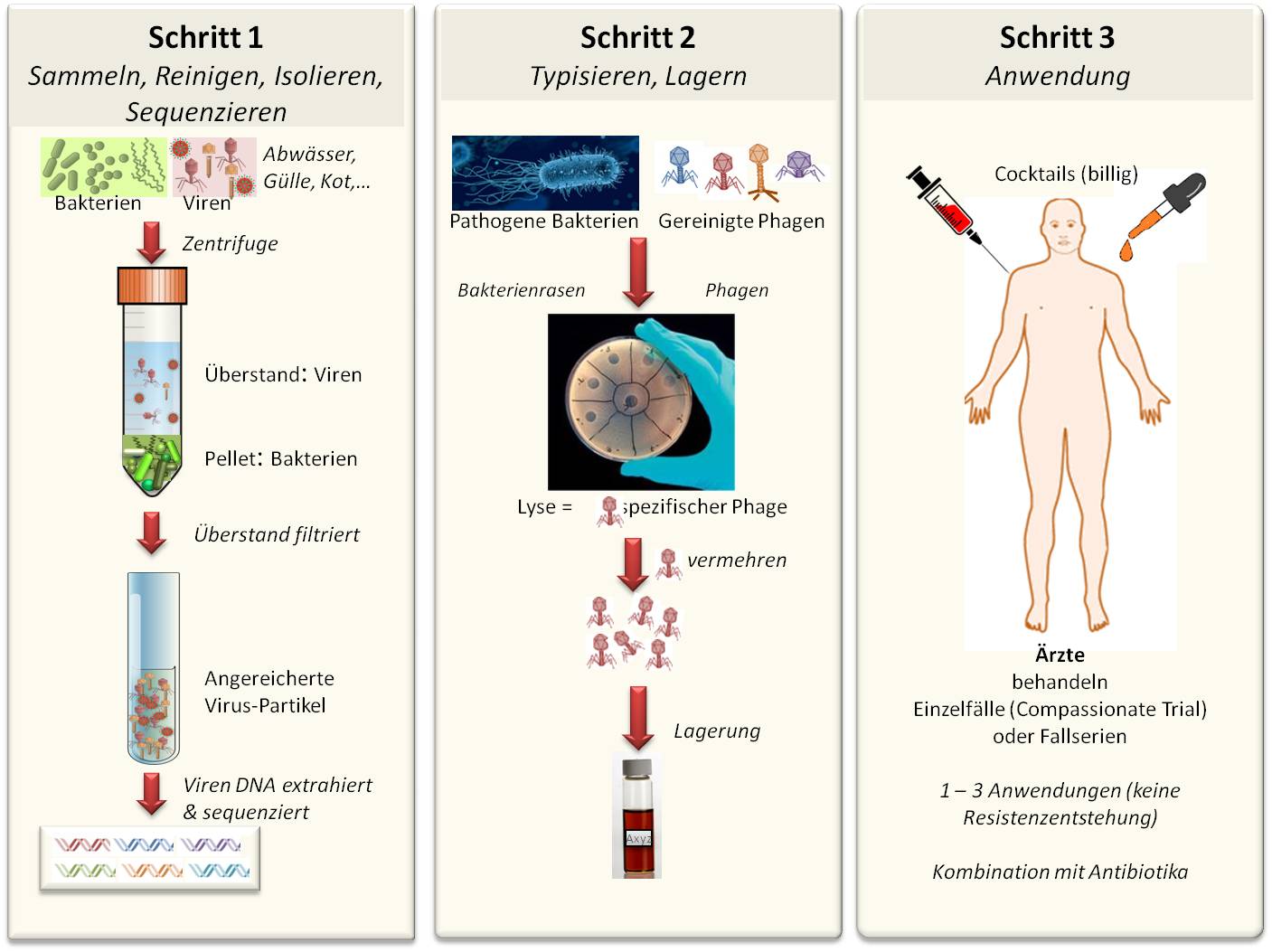 Abbildung 3. Vom Sammeln der Phagen zum Auffinden von spezifisch gegen Krankheitserreger wirkenden Phagen bis zu deren therapeutischer Anwendung.
Abbildung 3. Vom Sammeln der Phagen zum Auffinden von spezifisch gegen Krankheitserreger wirkenden Phagen bis zu deren therapeutischer Anwendung.
Im ersten Schritt werden Phagen gesammelt, gereinigt , isoliert und charakterisiert. Dazu werden Proben (u.a. aus Abwässern, Erde, Gülle, Kot,...) genommen, eventuell aufgeschlämmt und dann zentrifugiert, wobei die im Vergleich zu Phagen sehr großen Bakterien sedimentieren. Die im Überstand befindlichen Phagen und andere Viren werden angereichert, gereinigt, die unterschiedlichen Phagen isoliert und nach Vermehrung ihre DNAs auf die Base genau sequenziert.
Im zweiten Schritt werden potentielle Kandidaten zur Therapie auf Wirksamkeit getestet- typisiert. Dazu braucht es den jeweils richtigen Bakterientyp, an den Phagen spezifisch nach einem Schlüssel - Schloss-Prinzip andocken, ihr Erbgut in diesen Wirt injizieren, sich in ihm vermehren und ihn schließlich zur Lyse bringen (siehe [1]). Auf Kulturen von pathogenen Bakterien aufgebracht, beobachtet man, welcher Phagentyp Löcher in den dicht gewachsenen Bakterienrasen frisst, d.i. für den Krankheitserreger spezifisch ist und diesen lysiert. Solche spezifischen Phagen werden vermehrt, genau beschrieben und für den Anwendungsfall gelagert.
Die Anwendung schließlich muss von Ärzten durchgeführt werden: entweder als Einzelfallbehandlung (compassionate trial) oder neuerdings als Fallserie. Wie die immerhin seit einem Jahrhundert erfolgende Nutzung zeigt, sind bisher keine schweren Nebenwirkungen aufgetreten.
Dass schädliche bakterielle Komponenten oder Gene das Präparat möglicherweise verunreinigen und übertragen werden, kann verhindert werden indem hochgereinigte, gut charakterisierte und voll-sequenzierte Phagenprodukte angewandt werden. Ein solcher, nach der für Arzneimittel vorgeschriebenen "Good Manufacture Practice" (GMP) hergestellter, Phagencocktail wurde kürzlich im EU-Projekt Phagoburn zur Behandlung von mit Pseudomonas aeroruginosa infizierten Brandwunden angewandt.
Resistenzentwicklung gegen Phagen stellt auf Grund der hohen Spezifität für einen Bakterientyp und der Evolution des Phagen mit diesem Wirt ein wesentlich geringeres Risiko dar als es gegen Antibiotika der Fall ist; die Kombination Phage plus Antibiotikum senkt das Risiko noch weiter.
Eine Besonderheit der Phagentherapie ist, dass sie dosis-korrelliert ist und sich auch selbst limitiert: Je mehr Bakterien vorhanden sind, umso mehr Phagen werden in den Bakterien produziert. Sind alle Bakterien abgetötet, können sich die Phagen nicht mehr vermehren und gehen auch zugrunde. Abbildung 4.
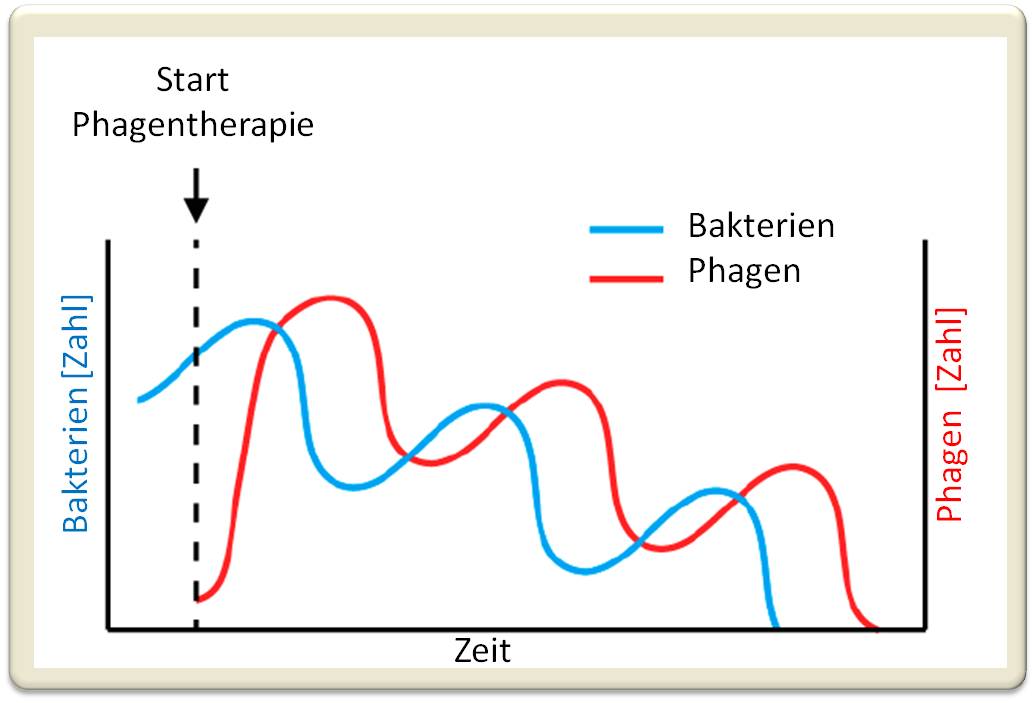 Abbildung 4. Schematische Darstellung der Populationsdynamik von Bakterien und Phagen während einer Phagentherapie. Phagen vermehren sich abhängig von der Bakteriendichte und nur so lange als Bakterien vorhanden sind.
Abbildung 4. Schematische Darstellung der Populationsdynamik von Bakterien und Phagen während einer Phagentherapie. Phagen vermehren sich abhängig von der Bakteriendichte und nur so lange als Bakterien vorhanden sind.
Neue rechtliche Bestimmungen
Offiziell ist in der westlichen Welt die Phagentherapie am Menschen nicht zugelassen, Ausnahmen sind Notfallverordnungen im Sinn der Helsinki Deklaration. Die nach wie vor geübte Anwendung in ehemaligen Ostblockstaaten wird erst im Licht westlicher Standards geprüft.
Phagen sind Biologika, welche in den (bereits veralteten) Richtlinien der Zulassungsbehörden in der EU und den USA noch nicht berücksichtigt sind. Daher können sie die strengen Anforderungen hinsichtlich Standardisierung und Reproduzierbarkeit nicht erfüllen, die einst für synthetische Wirkstoffe, Impfstoffe, Proteine, etc. formuliert worden sind. Diese verlangen ein genau definiertes, identisches Ausgangsmaterial, was bei Phagen nicht möglich ist, wenn man diese spezifisch auf die Keime jedes einzelnen Patienten abstimmt. Ist andererseits eine breitere Anwendung vorgesehen (beispielsweise zur Behandlung von Epidemien) und daher eine große Menge eines Phagenpräparats erforderlich, so kann dieses infolge von Mutation während der Herstellung uneinheitlich werden und damit die geforderte "Good Manufacture Practice" (GMP) fehlschlagen lassen.
Sofern es sich um eine personalisierte Therapie handelt, bietet die sogenannte Magistrale-Anwendung einen Ausweg, der bereits in Belgien praktiziert werden darf: hier kann der Arzt ein Phagen-Präparat verordnen, das passgenau auf einen Patienten mit einem bestimmten Keim zugeschnitten ist und ganz individuell in der Krankenhaus-Apotheke hergestellt wird.
Ein massives Problem der Phagentherapie besteht weiters darin, dass der akzeptierte Entwicklungsprozess von Arzneimitteln eine klinische Prüfung vorsieht , in welcher die Wirkung eines Wirkstoffs auf ein Target (eine Zielstruktur) geprüft wird. Dies ist bei hochspezifischen Phagen problematisch, da ja meistens mehrere Targets vorliegen und für jedes Target mehrere Phagen - ein Phagencocktail - eingesetzt werden müssen.
Um Phagentherapie rasch einsetzen zu können, braucht es also einen neuen rechtlichen Rahmen für medizinische Produkte, der Phagen mit ihren Besonderheiten mit einbezieht.
Systematische Studien
Die lange Erfahrung und die erfolgreichen Anwendungen der Phagentherapie in den ehemaligen Ostblockländern werden von westlichen Behörden als nicht ausreichend dokumentiert angesehen und als zu wenig überzeugend was die Wirksamkeit und ein mögliches Auftreten schwerer Nebenwirkungen betrifft. Um eine breite sichere Anwendung der Phagen-Therapie zu gewährleisten, müssen zahlreiche systematische klinische Studien vorliegen, die dann eine Grundlage für die Zulassungsbehörden bieten, um Richtlinien für die Phagentherapie zu erstellen.
Es kann noch Jahre dauern bis es soweit ist. Bis dahin können Patienten auf eigenes Risiko und eigene Kosten nach Georgien oder Polen pilgern, wo Phagentherapie routinemäßig durchgeführt wird (eine 3-wöchige Behandlung gegen multiresistenten Staphylococcus aureus kommt auf etwa 5 000 €).
[1] Karin Moelling, 04.07.2019: Viren gegen multiresistente Bakterien. Teil 1: Was sind Phagen?
[2] No Time to Wait: Securing the future from drug-resistant infections. (April 2019). Report to the Secretary-General of the United Nations.
[3] EU Action on Antimicrobial Resistance.
Weiterführende Links
Karin Moelling, Felix Broecker, Christian Willy (12.2018): A Wake-Up Call: We Need Phage Therapy Now. Viruses 2018, 10, 688; doi:10.3390/v10120688
Karin Moelling (10.2017): Viren statt Antibiotika.
Karin Moelling: Welt der Viren, 2. Phagen (2015); Video 9:22 min.
Karin Moelling: Ohne Viren gäbe es schlicht kein Leben. Virologin Prof. Dr. Karin Mölling zu Gast bei KKL Impuls (2016), Video 1:17:05 min.
Karin Moelling: Collect Phages to Kill resistant Bacteria (deutsch). 2019; Video 12:14 min.
Karin Moelling: Tischgespräche (24.07.2019), Podcast 52:41 Min
Karin Moelling: New Case Reports with Phage Therapy-What is Needed for More? (2019). Nursing and Health Care 4:30-32
William C. Summers (2016) Félix Hubert d'Herelle (1873–1949): History of a scientific mind, Bacteriophage, 6:4, e1270090, DOI: 10.1080/21597081.2016.1270090
UC San Diego Health (2017): Phage Treatment Saves A Life. Video 5:57 min. (Der Tom Patterson Fall)
Phage Therapy: An Effective Alternative to Antibiotics? Video 10:58 min. The Eliava Institute in Georgia is the world leader in phage production. Patients travel from all around the world for treatment.
Udo Pollmer: Bakteriophagen - natürlicher Ersatz für Antibiotika und Desinfektion? 2013; Video 7:38 min.
DSMZ: The Life Cycle of Bacteriophages. Video 3:18 min.
A.Gorski et al., (2018): Phage Therapy: What Have We Learned? Viruses; 10(6): 288. doi: 10.3390/v10060288