Wie verläuft eine Corona-Infektion? Ergebnisse der ersten Human-Challenge-Studie
Wie verläuft eine Corona-Infektion? Ergebnisse der ersten Human-Challenge-StudieSa 12.02.2022 — Inge Schuster

![]() Wesentliche Fragen zu Übertragung und Verlauf der Infektion mit SARS-CoV-2 konnten bislang nicht geklärt werden. Aus der ethisch umstrittenen britischen Challenge-Studie konnten erstmals konkrete Aussagen über den gesamten Verlauf der Infektion, insbesondere über deren frühe Phasen und Infektiosität getroffen werden, die in die Überlegungen zu verbesserten Teststrategien einfließen sollten. In dieser Studie wurden 34 junge, gesunde Probanden mit einer sehr niedrigen Dosis des Coronavirus (einer "prä-alpha" Variante) inokuliert, wovon 18 Probanden eine Infektion davontrugen, die zu vorübergehenden, leichten bis mittelschweren Symptomen führte. Es zeigte sich, dass früher als bisher angenommen (aktives) Virus im Rachenraum und dann in den Nasenhöhlen detektierbar wird und damit die Infektiosität - für die ein Nasentröpfchen reicht - früher als erwartet einsetzen kann, dass es sehr schnell zu einem sehr hohen Anstieg der Viruslast vor allem in der Nase kommt und Symptome offensichtlich nicht direkt mit der Viruslast korreliert sind. Besonders erwähnenswert: Die Infektion führt bei einem hohen Anteil auch junger, gesunder Menschen zu (sehr) lang anhaltenden Beeinträchtigungen des Geruchsinns: In dieser Studie waren zwei Drittel der Infizierten davon betroffen.
Wesentliche Fragen zu Übertragung und Verlauf der Infektion mit SARS-CoV-2 konnten bislang nicht geklärt werden. Aus der ethisch umstrittenen britischen Challenge-Studie konnten erstmals konkrete Aussagen über den gesamten Verlauf der Infektion, insbesondere über deren frühe Phasen und Infektiosität getroffen werden, die in die Überlegungen zu verbesserten Teststrategien einfließen sollten. In dieser Studie wurden 34 junge, gesunde Probanden mit einer sehr niedrigen Dosis des Coronavirus (einer "prä-alpha" Variante) inokuliert, wovon 18 Probanden eine Infektion davontrugen, die zu vorübergehenden, leichten bis mittelschweren Symptomen führte. Es zeigte sich, dass früher als bisher angenommen (aktives) Virus im Rachenraum und dann in den Nasenhöhlen detektierbar wird und damit die Infektiosität - für die ein Nasentröpfchen reicht - früher als erwartet einsetzen kann, dass es sehr schnell zu einem sehr hohen Anstieg der Viruslast vor allem in der Nase kommt und Symptome offensichtlich nicht direkt mit der Viruslast korreliert sind. Besonders erwähnenswert: Die Infektion führt bei einem hohen Anteil auch junger, gesunder Menschen zu (sehr) lang anhaltenden Beeinträchtigungen des Geruchsinns: In dieser Studie waren zwei Drittel der Infizierten davon betroffen.
Nach nunmehr 2 Jahren Corona-Pandemie mit nahezu 400 Millionen Infizierten, über 5,7 Millionen an/mit COVID-19 Verstorbenen und einem bisher nie dagewesenen globalen Forschungsaufwand, der uns neuartige, hochwirksame Vakzinen und wirksame antivirale Medikamente bescherte, sind wesentliche Fragen zu Übertragung und Verlauf der Infektion bislang ungeklärt geblieben. Eine sogenannte Human-Challenge-Studie sollte hier Einblick schaffen, d.i. eine Studie, bei der gesunde Menschen gezielt dem Virus ausgesetzt werden, um Zeitverlauf (die Kinetik) der Infektion, Viruslast, Infektiosität und Krankheitssymptome quantitativ erfassen zu können. In weiterer Folge lässt sich dann untersuchen, wieweit eine Infektion durch Impfstoffe oder Medikamente unterdrückt werden kann. Mit einer relativ kleinen Zahl an Studienteilnehmern kann so zeit-und kostensparend zwischen potentiellen Vakzinen/Medikamenten selektiert und optimiert werden. Die erste derartige Challenge Studie mit SARS-CoV-2 startete im März 2021 in Großbritannien, ihre (vorläufigen) Ergebnisse wurden vorige Woche auf einem preprint Server von Springer Nature publiziert (sind also noch nicht peer-reviewed) [1].
Ethische pros und cons
Human-Challenge-Studien konnten bereits in der Vergangenheit die Entwicklung von Therapien in anderen Infektionskrankheiten, wie Typhus, Cholera, Malaria und Influenza wesentlich vorantreiben [2] - als ältestes Beispiel kann wohl die Geburtsstunde der Vakzinologie - die 1798 von Edward Jenner durchgeführte Impfung mit Kuhpocken - gesehen werden, die schlussendlich zur Ausrottung der Pocken führte. Solche Studien werden heute vom ethischen Standpunkte aus kontrovers diskutiert: einem für die öffentliche Gesundheit äußerst wertvollen Erkenntnisgewinn steht das vielleicht sehr hohes Risiko gegenüber gesunde freiwillige Probanden schwerkrank zu machen. Dabei werden freilich Erinnerungen an verbrecherische Untersuchungen auch aus jüngerer Zeit wach, die an Personen ohne deren Information und Einverständnis stattfanden - Häftlinge, Kriegsgefangene, aber auch geistig zurückgebliebene Patienten in psychiatrischen Anstalten waren die bedauernswerten Opfer.
Auch im Vorfeld der Human Challenge Studien mit SARS-CoV-2 hat es ernste Bedenken gegeben, beispielsweise hat John Mascola, Direktor am NIH-Vaccine Research Center (VRC), im Juli 2020 dazu geäußert: "Für Challenge-Studien wäre es vorzuziehen, eine sehr wirksame Behandlung mit synthetischen Arzneimitteln oder Antikörpern zur Hand zu haben. Wenn jemand krank wird, kann man sehr schnell mit den Behandlungen gegen die Infektion beginnen. Wir haben keine kurativen Behandlungen, daher sind wir derzeit noch nicht für COVID-19-Challenge-Studien gerüstet"[3].
Tatsächlich war damals erst eine einzige antivirale Substanz - Remdesivir - zur Behandlung zugelassen, die sich später in zahlreichen Studien allerdings als wenig bis völlig unwirksam herausstellen sollte (so auch in der Challenge-Studie, s. Abbildung 2). Ab Dezember 2020 stand dann auch ein Antikörpercocktail von Regeneron zur Verfügung, der vor schweren Krankheitsverläufen schützen sollte (auch Präsident Trump wurde damit behandelt).
Die britische Challenge-Studie
Bereits im Oktober 2020 kündigte ein britisches Forscherteam die erste Human-Challenge-Studie mit dem Coronavirus an. Das Versuchsprotokoll sah eine streng kontrollierte klinische Untersuchung unter Quarantänebedingungen an jungen gesunden Freiwilligen vor, die mit einer definierten niedrigen Dosis eines gut charakterisierten Virus infiziert werden sollten. Die Ethikkommission der UK Health Research Behörde genehmigte im Feber 2021 die den internationalen Ethikrichtlinien (incl. der Helsinki-Deklaration) genügende Studie und diese startete im März 2021, finanziert von der britischen Regierung mit rund 40 Millionen €. Unter der Leitung des Imperial College London waren mehrere britische Forschungsinstitutionen daran beteiligt, in Partnerschaft mit dem kommerziellen Unternehmer hVIVO Services Ltd.(Teil von Open Orphan), der weltweit als Pionier und führender Experte für das Testen von Impfstoffen und antiviralen Medikamenten in Human Challenge-Studien gilt.
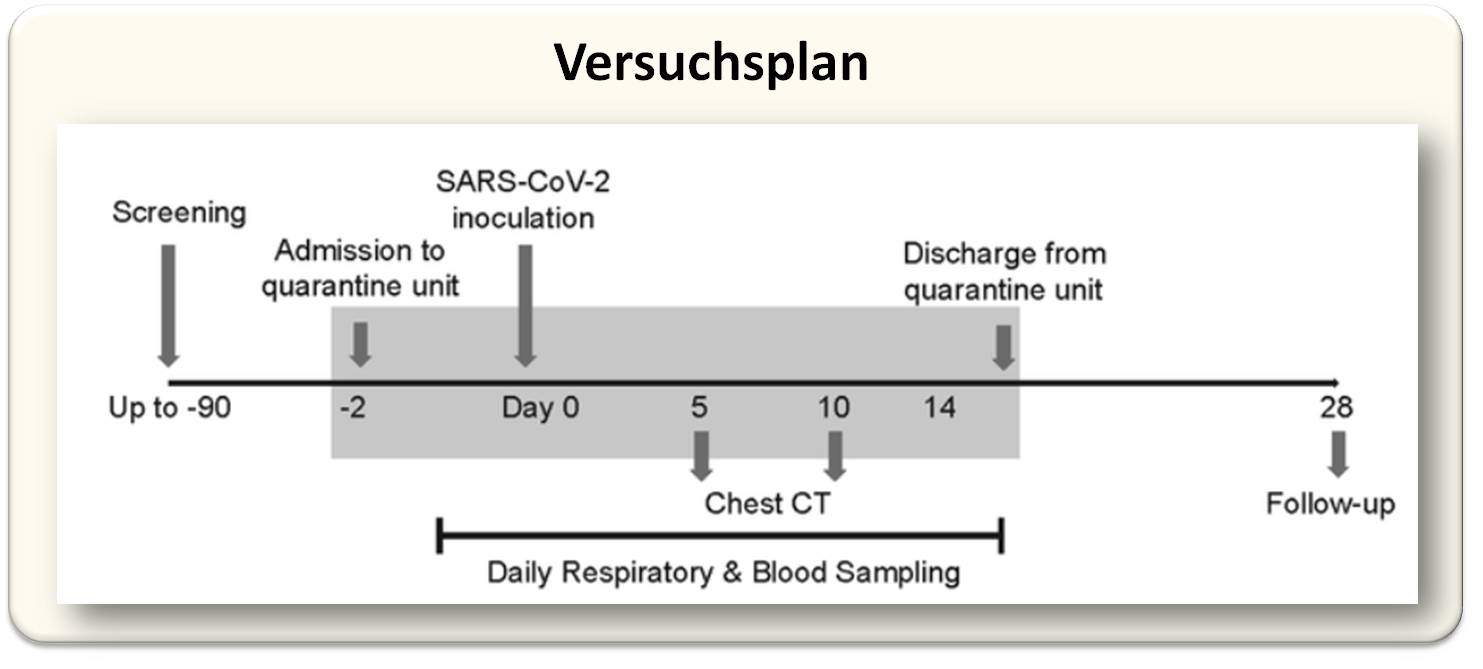
Das Interesse an der Studie war groß, nahezu 30 000 Personen registrierten sich als potentielle Teilnehmer; von diesen wurden in einem Screening-Verfahren 34 junge, gesunde Personen (26 Männer, 8 Frauen) im Alter von 18 - 29 Jahren ausgewählt; diese hatten noch keine SARS-CoV-2 Infektion hinter sich und waren auch nicht dagegen geimpft. Das Design der Studie ist in Abbildung 1 skizziert
| Abbildung 1: Design der klinischen Challenge Studie. Bild aus Ben Killingley et al., [1]. Lizenz cc-by 4.0. |
Bereits 2 Tage vor der Infektion mit dem Virus bezogen die Freiwilligen Einzelzimmer mit 24stündiger medizinischer Überwachung in der Quarantänestation des Royal Free London NHS Foundation Trust. Die Inokulation mit dem Virus erfolgte in die Nasenhöhle mit einem Tröpfchen der niedrigsten noch quantifizierbaren Dosis einer Variante, die noch weitgehend dem ursprünglichen Wildtyp entsprach ("prä-Alpha-Variante). Täglich zweimal entnommene Nasen-und Rachenabstriche (in jeweils 3 ml Medium) ermöglichten Infektionsverlauf und Viruslast zu bestimmen. Auftretende Symptome haben die Probanden 3 x täglich in einem Tagebuch notiert. Zur Sicherheit der Probanden wurden tägliche Bluttests, Lungenfunktionstests, Tests auf diverse klinische Parameter, EKGs und Thorax-CTs durchgeführt. Beeinträchtigungen des Geruchsinns wurden mittels des von der University of Pennsylvania entwickelten Smell Identification Tests (UPSITs) festgestellt. Die Probanden blieben mindesten 14 Tage nach Inokulation in Quarantäne und wurden erst entlassen, wenn an 2 aufeinanderfolgenden Tagen kein Virus in den Nasen-/Rachen-Abstrichen mehr nachweisbar war. Weitere Tests erfolgten nach 28 Tagen und sollen auch noch nach einem Jahr stattfinden.
Als Kompensation für die Teilnahme an der Studie wurden 4500 Pfund pro Proband vorgesehen.
Der Infektionsverlauf
Erstmals konnte ein Einblick in die Anfangsphase der Infektion gewonnen werden, d.i. wie lang es nach dem definierten Zeitpunkt der Inokulation dauert bis Virusausscheidung detektierbar wird, Infektiosität eintritt (Latenzzeit) wie schnell und wie hoch die Virenlast ansteigt und wann es zu Symptomen kommt (Inkubationszeit).
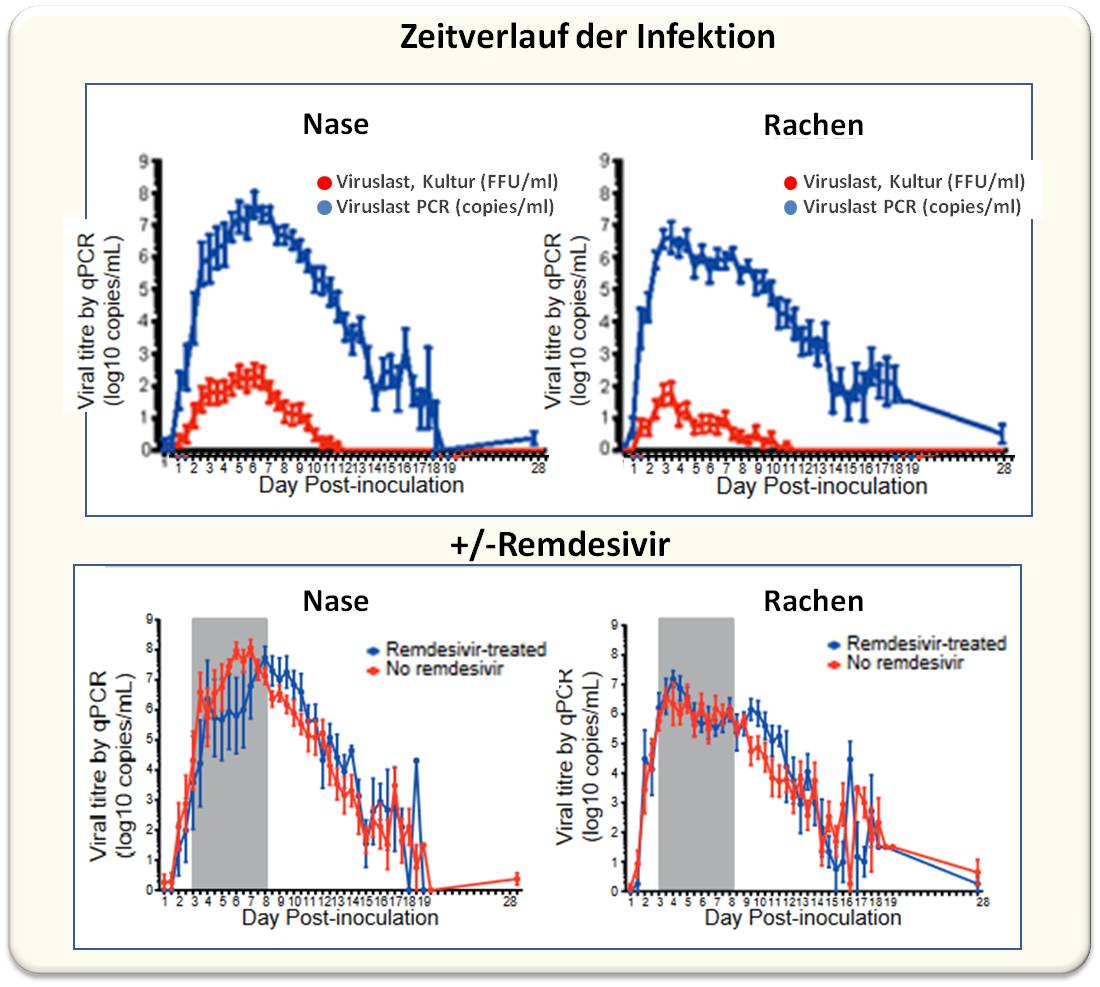
| Abbildung 2: Zeitverlauf der Viruslast in Nasen-und Rachenabstrichen. Oben: Bestimmung der Viruslast mittels PCR-Test in Kopien des Nucleocapsid-Gens/ml (blau) und mittels Test auf funktionelles Virus in Kultur in Foci-bildenden Einheiten (FFU)/ml (rot). Unten: Die präventiv verabreichte antivirale Substanz Remdesivir (blau) kann weder die Viruslast reduzieren noch den Zeitverlauf beeinflussen. Die Viruslast ist logarithmisch dargestellt in Form von Mittelwerten+/- Standardabweichung. Bild modifiziert aus Ben Killingley et al., [1]. Lizenz cc-by 4.0. |
Das niederdosierte Inokulum des vermehrungsfähigen Virus (5,5 Mio Kopien/ml, 55 FFU/ml) führte bei 18 der 34 Probanden zur Infektion (das entsprach der angepeilten Inzidenz von 50 %). Bereits früher als man bislang angenommen hat, wurde Virusausscheidung in Nase und Rachen detektierbar: mittels PCR-Test (auf das Nucleocapsid-Gen) und auch mittels des Foci-Forming Tests in Zellkultur auf aktives Virus wurde die Viruslast im Rachen bereits nach 40 Stunden, in der Nase nach 58 Stunden nachgewiesen. Die Virusmengen stiegen dann rasant an, erreichten einen Maximalwert im Rachen von im Mittel 65 Mio Kopien/ml (800 FFU/ml) nach rund 4,7 Tagen und einen um eine Größenordnung höheren Wert von 750 Mio Kopien/ml (8000 FFU/ml) in der Nase nach 6,2 Tagen. Abbildung 2.
Auch der weitere Infektionsverlauf brachte eine neue Erkenntnis: Die Virusausscheidung klang nur langsam ab - auch 14 Tage nach Inokulation war bei allen Infizierten das Virus noch quantifizierbar, sodass bis zur fehlenden Detektierbarkeit die Quarantäne noch bis zu 5 Tage länger andauern musste.
Remdesivir erweist sich als wirkungslos
In der Hoffnung mit dem antiviralen Medikament Remdesivir den Infektionsverlauf beeinflussen zu können, wurden 10 Teilnehmer präventiv - sobald das Virus in den Abstrichen detektierbar wurde - über 5 Tage mit täglich 200 mg der Substanz behandelt. Weder der Zeitverlauf noch die Höhe der Viruslast zeigten einen Unterschied zu den nicht mit Remdesivir Behandelten (Abbildung 2). Auch hinsichtlich der Symptome gab es keinen Unterschied.
Bildung von Antikörpern
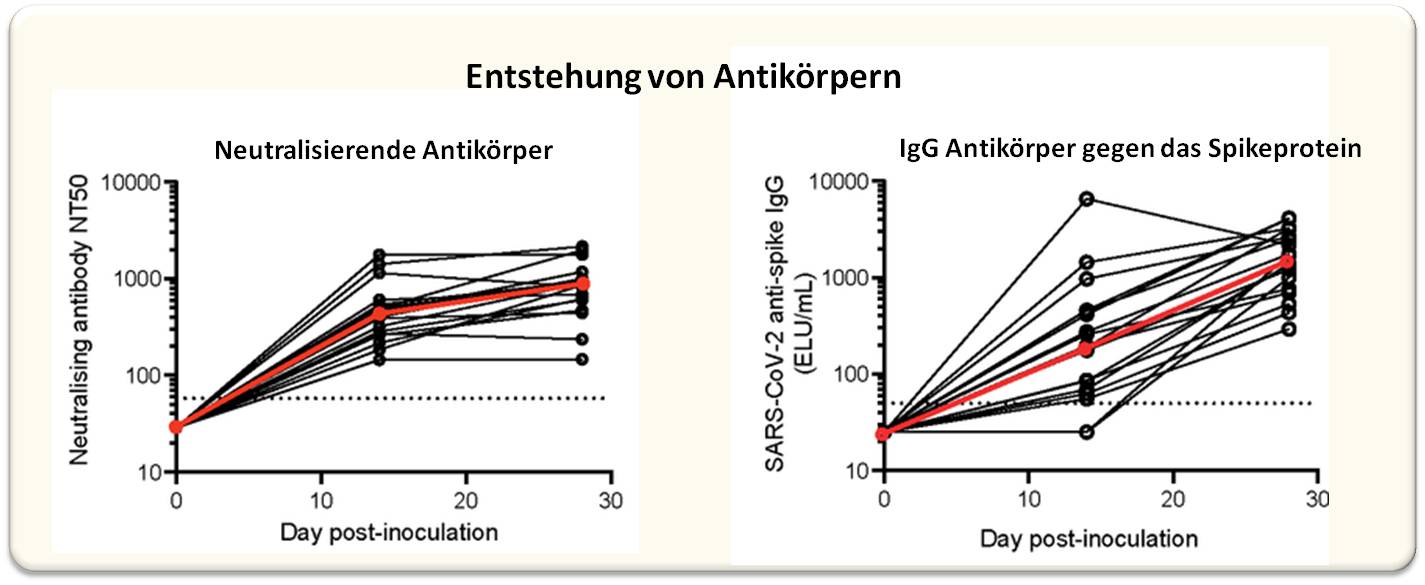
In allen infizierten Probanden hat das Immunsystem mit der Bildung von Virus-neutralisierenden - also vor der Vermehrung des Virus schützenden - Antikörpern geantwortet. Gesamt gesehen stieg deren Serumspiegel in den ersten beiden Wochen nach Infektion rasch an, um sich dann bis zum 28. Tag nur mehr zu verdoppeln. Abbildung 3. Speziell gegen das Spikeprotein, mit dem das Virus an unsere Zellen andockt, entstanden Antikörper wesentlich langsamer und zeigten dabei große individuelle Unterschiede im Zeitverlauf. Im Mittel erfolgte dann zwischen 14. und 28. Tag nach Infektion ein Anstieg der Spikeprotein- Antikörper auf das 10-fache.
| Abbildung 3: Neutralisierende Antikörper (links, gemessen im Serum mittels Mikroneutralisationstest; NT50: Verdünnung des Serums bei der die Virusvermehrung in der Zellkultur um 50 % reduziert wird) und Antikörper speziell gegen das virale Spikeprotein (rechts). Bild modifiziert aus Ben Killingley et al., [1]. Lizenz cc-by 4.0. |
Symptome
Von den 18 Infizierten entwickelten 16 Symptome, die sich 2 - 4 Tage nach Infektion bemerkbar machten. Es gab keine schweren Erkrankungen, keine Veränderungen der Lunge. Der Antikörpercocktail (Regeneron), der zur Behandlung schwerer Fälle hätte dienen können, brauchte nicht eingesetzt werden.
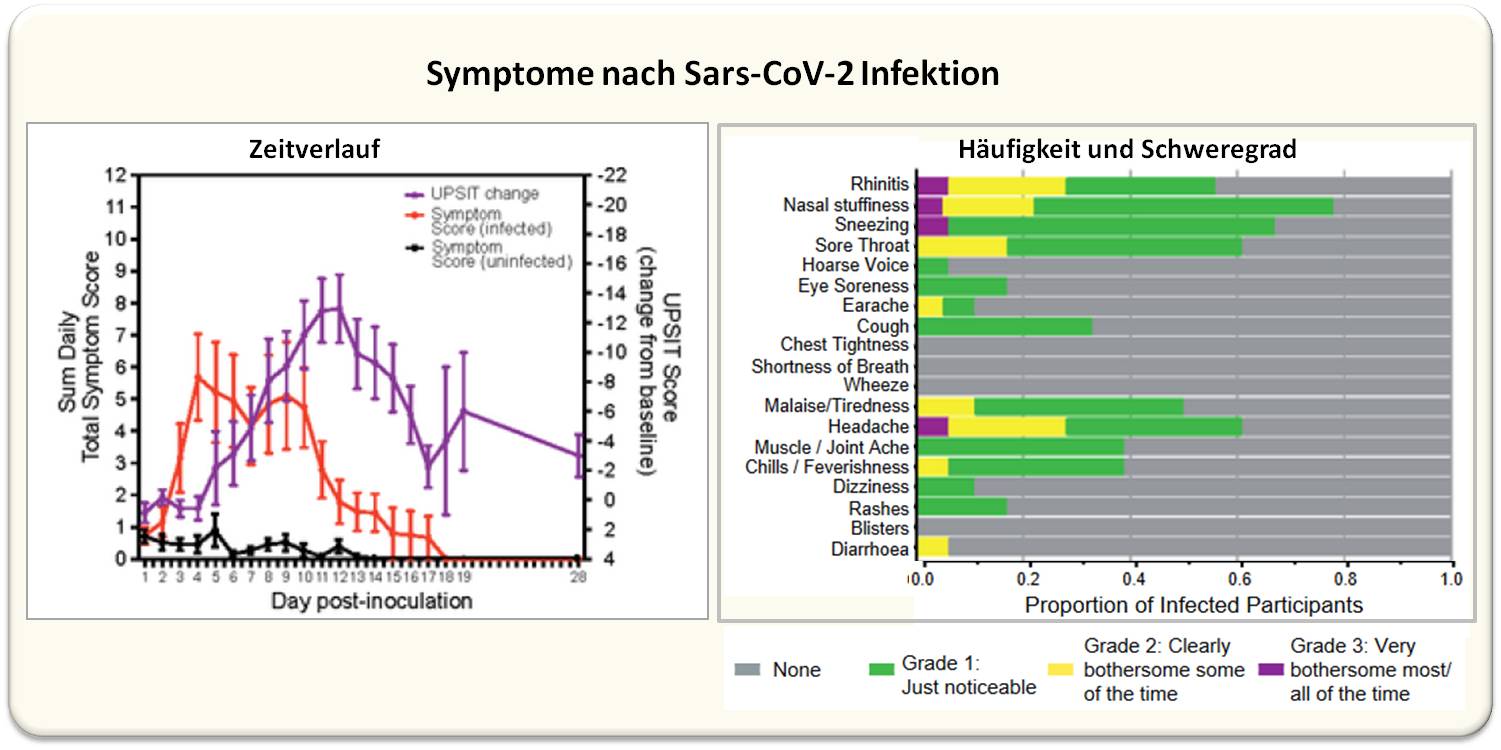
Trotz der stark ansteigenden, sehr hohe Titer erreichenden Virusausscheidung in Nase und Rachen, waren die Symptome leicht bis mittelschwer und zum überwiegenden Teil Erkältungssymptomen ähnlich. Sie betrafen vor allem den oberen Atmungstrakt - verstopfte/rinnende Nase, trockene Kehle - waren aber auch systemisch - Fieber, Muskel-/Gelenksschmerzen, Kopfschmerzen - anzutreffen. Abbildung 4 (rechts).
Ein für COVID-19 charakteristisches Symptom ist die Beeinträchtigung des Geruchsinns. Diese trat bei zwei Drittel (12/18) der infizierten Probanden (nicht aber bei den Nichtinfizierten) auf, bei 9 davon (50 %) kam es zu völligem Riechverlust. Riechminderung/Riechverlust setzte wesentlich später ein als die anderen Symptome und blieb auch länger bestehen (Abbildung 4, lila Kurve). Am Tag 28 berichteten noch 11 Probanden über Beeinträchtigungen, nach 90 Tagen waren es 4 und 5 nach 180 Tagen (Table 1, [1]).
Nach Ablauf eines Jahres sollen die Probanden nochmals auf potentielle Langzeitfolgen der Infektion untersucht werden.
| Abbildung 4: Die Infektion mit SARS-CoV-2 hat zu häufigen milden, bis mittelschweren Symptomen geführt, die mit dem Zeitverlauf nicht aber mit der Höhe der Viruslast in Nase und Rachen (siehe Abbildung 2) korrelieren . Dies ist insbesondere für den sehr häufig auftretenden Riechverlust der Fall. Links: Gesamtscore der Symptome der Infizierten (rot), Riechverlust (lila, gemessen mittels University of Pennsylvania Smell Identification Tests - UPSIT). Gesamtscore der Symptome der Nichtinfizierten (schwarz). Bild aus Ben Killingley et al.,[1]. Lizenz cc-by 4.0. |
Ausblick
Die Challenge-Studie hat gezeigt, dass ein sehr niedriges, gerade noch quantifizierbares Inokulum des aktiven Virus ausreicht, um eine Infektion hervorzurufen. Derartig niedrige Virusmengen können bereits in frühen Infektionsphasen in einem einzigen Nasentröpfchen, in einem Atemlufttröpfchen vorhanden sein, Infizierte früher als angenommen ansteckend sein. (Demzufolge erweist sich wiederum die Mund-Nasenmaske als besonders wirksame Schutzmöglichkeit) Eine wesentliche Frage ist, warum einige Menschen angesteckt werden und andere nicht. Um herauszufinden, welche Faktoren Schutz bieten können, wertet das Forscherteam der Challenge-Studie eine Fülle weiterer Ergebnisse aus, analysiert lokale und systemische immunologische Marker, darunter mögliche kreuzreaktive Antikörper, T-Zellen und lösliche Mediatoren (Cytokine) und molekularbiologische Parameter wie Genexpression.
In Hinblick auf sogenannte Impfdurchbrüche will das Forscherteam in weiteren Challenge-Studien vormals infizierte und geimpfte Probanden mit steigenden Dosierungen des Wildtyps und/oder mit anderen Virusvarianten zu inokulieren, um herauszufinden, welche Faktoren zu einem klinischen Befund führen.
In Zukunft können Challenge-Studien eine Plattform bieten, um im frühen Entwicklungsstadium schnell und effizient antivirale Entwicklungssubstanzen, Impfstoffkandidaten und Diagnostika auf Eignung zu testen und Studien zu vermeiden, die auf einer kontinuierlichen Übertragung der Infektion in der Gemeinschaft beruhen.
-----------------------------------------
Nachsatz (I.S.)
Mit Ausnahme des gestörten Riechsinns hat die Challenge-Studie rasch vorübergehende leichte bis mittelschwere Symptome hervorgerufen. Minderung bis hin zum Verlust des Riechsinn, von dem 2/3 der Infizierten betroffen war, gehört zu dem sehr häufig auftretenden, noch weithin unverstandenen Kranheitsbild von long-COVID, das eine erhebliche Reduzierung der Lebensqualität mit sich bringt [4]. Weitere Challenge-Studien, vor allem auch mit aggressiveren Virus-Varianten, sollten erst starten, wenn man in der Lage ist die langzeitigen negativen Folgen für die jungen, geunden Probanden zu minimieren.
[1] Ben Killingley et al., Safety, tolerability and viral kinetics during SARSCoV-2 human challenge. (posted 1. Feb. 2022) https://doi.org/10.21203/rs.3.rs-1121993/v1
[2] Euzebiusz Jamrozik and Michael J. Selgelid: History of Human Challenge Studies. Human Challenge Studies in Endemic Settings . 2021 : 9–23. doi:10.1007/978-3-030-41480-1_2
[3] Francis S. Collins. 16.07.2020: Fortschritte auf dem Weg zu einem sicheren und wirksamen Coronaimpfstoff - Gepräch mit dem Leiter der NIH-COVID-19 Vakzine Entwicklung
[4] Inge Schuster, 7.1.2022:Was ist long-COVID?
Artikel in ScienceBlog.at
Zu COVID19 sind bis jetzt 42 Artikel erschienen. Die Links finden sich zusammengefasst unter: Themenschwerpunkt Viren